7月15日,南京医科大学基础医学院细胞生物学系、卫健委抗体技术重点实验室汪秀星课题组与匹兹堡大学医学中心Jeremy Rich课题组、中山大学第一附属医院神经外科张弩课题组合作在肿瘤研究杂志《Cancer Research》上发表了题为“β2-microglobulin maintains glioblastoma stem cells and induces M2-like polarization of tumor-associated macrophages” 的研究论文,该研究揭示了胶质瘤干细胞干性维持及其肿瘤微环境调控的新机制,为胶质母细胞瘤的临床治疗新策略提供理论基础。

胶质母细胞瘤(GBM)是恶性程度和致死率最高的中枢神经系统肿瘤。病人平均生存期仅有14-16个月,五年生存率不足10%。目前除了手术及放化疗外,并无有效治疗方法。GBM内的胶质瘤干细胞(glioblastoma stem cells,GSCs)是造成GBM高恶性程度、治疗抵抗与复发的关键,GSCs是存在于肿瘤内具有自我更新功能、驱使肿瘤形成的一类细胞。GBM肿瘤微环境中GSCs与肿瘤相关巨噬细胞(TAMs)相互作用进一步促进了肿瘤的恶性进展。因此,探讨GSCs与TAMs的调控机制有利于深入阐明GBM发病机制。
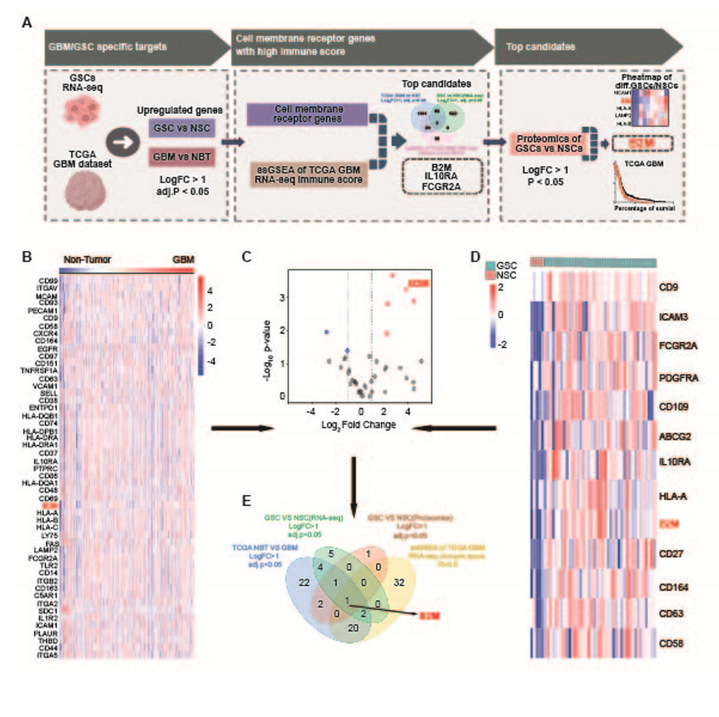
研究通过联合转录组学、蛋白质组学以及癌症基因组图谱计划(TCGA)数据库等多组学分析发现主要组织相容性复合体I类分子(MHC-I)的重要组成部分β2-微球蛋白(beta 2-microglobulin, B2M)特异性高表达于GSCs与GBM病人脑肿瘤样本,通过细胞功能与动物模型验证了B2M在维持GSCs干性及肿瘤微环境调控中发挥重要作用。
研究发现,B2M结合跨膜蛋白PIP5K1A激活 PI3K/AKT 信号维持GSCs自我更新与肿瘤发生;同时,B2M作为 M2 样 TAMs 维持的调节因子,通过调节GSCs的PI3K/AKT-MYC-TGF-β1信号轴,诱导TGF-β1分泌,激活TAMs的旁分泌SMAD和PI3K/AKT信号,从而促进M2样TAMs的免疫抑制作用。该研究提示靶向B2M或其下游信号轴将为治疗GBM提供新途径。
南京医科大学基础医学院细胞生物学系硕士研究生李大奇、国家卫健委抗体技术重点实验室助理研究员张茜为该工作共同第一作者,南京医科大学汪秀星教授、美国UPMC Jeremy N. Rich以及中山大学第一附属医院张弩教授为共同通讯作者。课题还获得了南京医科大学第一附属医院神经外科尤永平主任、南京医科大学生殖国家重点实验室李朝军教授等多位合作者的指导和支持。本课题由国家重大人才工程青年项目、国家重点研发计划、国家自然基金委项目资助。
(素材/汪秀星课题组;审核/王晓明)